摘要
- 2022年8月底開始,網絡流傳聲稱來自英國政府網站截圖及連結,指當地於今年8月中修改接種復必泰疫苗指引,從原來顯示懷孕及哺乳婦女可接種,改為無法為孕婦安全使用提供足夠保證,哺乳婦女亦不應接種。
- 查證發現,該截圖及連結屬2020年12月復必泰在英國取得臨時上巿許可的相關文件,非接種疫苗的長期指引。對上一次更新日期為2021年6月,並非今年8月,修改的內容亦與孕婦、哺乳等部分無關。
- 文件註明就生育、懷孕及哺乳應否接種疫苗說法,只反映當時缺乏充分數據下的建議。
- 英國政府自2021年4月正式建議孕婦接種COVID-19,亦有引用數據及研究顯示無負面影響。
- 網絡另流傳文章引述其他英國政府文件質疑孕婦接種疫苗安全性,經查證後確認為舊資料,現已不適用。
- 網傳訊息將英國政府舊資料稱為今年8月中更新疫苗指引,以該文件質疑婦女生育、懷孕及哺乳接種COVID-19疫苗不安全,屬錯誤訊息。
背景
2022年8月30日,Facebook專頁「白兵 Stormtrooper」發佈一張來自Twitter用戶「Nikki」(@nikki_miumiu)帖文的截圖,並在留言附上該帖文連結。[1,2]《熱血時報》網台節目主持陳秀慧亦在Facebook轉載來自「Nikki」的訊息。[3]兩則Facebook帖文共獲680個表情回應、51個留言及171次分享。
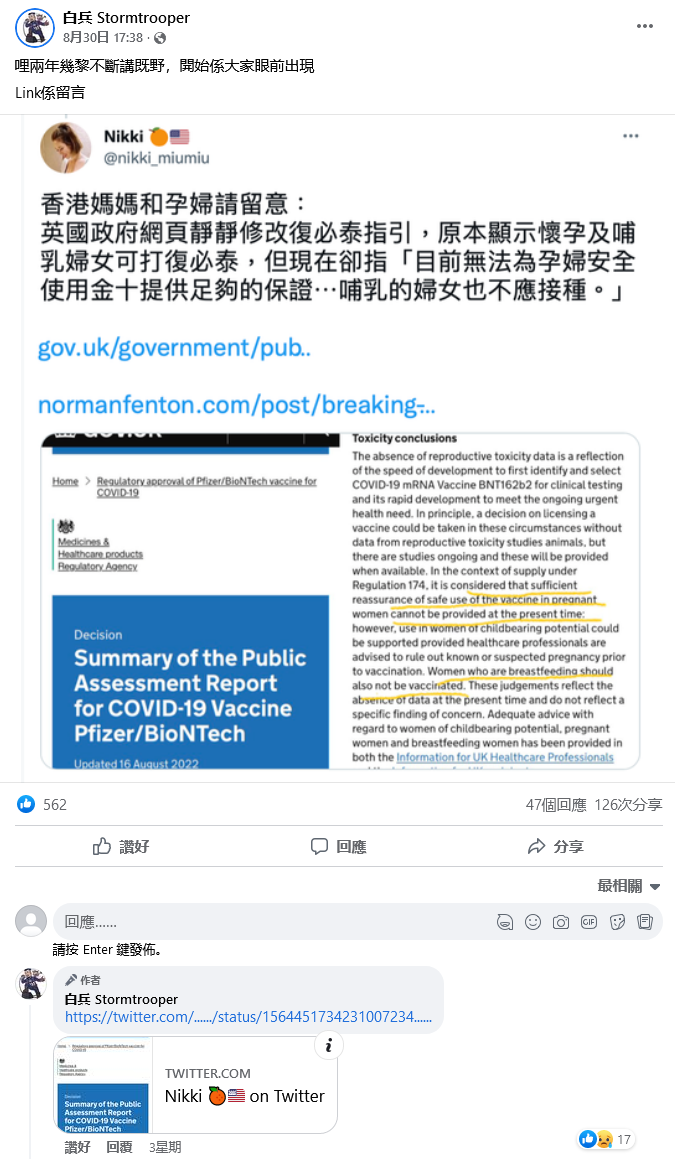
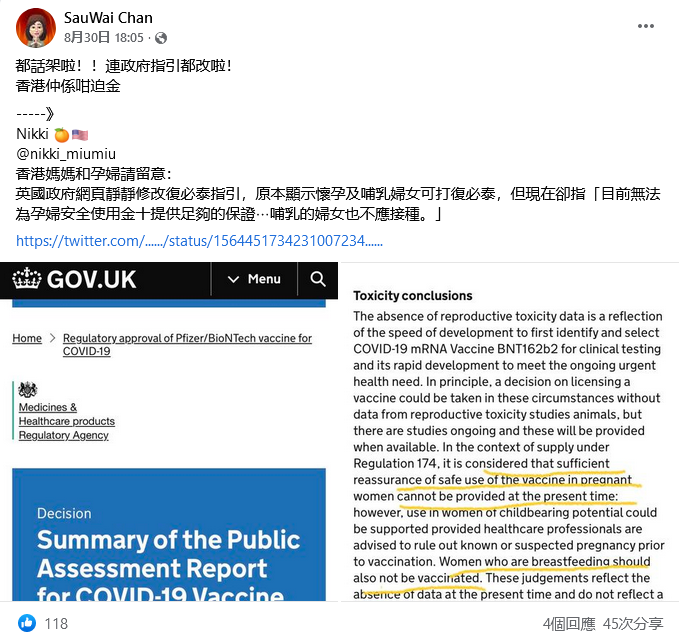
「Nikki」的帖文宣稱「英國政府網頁靜靜修改復必泰指引,原本顯示懷孕及哺乳婦女可打復必泰,但現在卻指『目前無法為孕婦安全使用金十提供足夠的保證⋯哺乳的婦女也不應接種』」(原文以「金十」借代「針」,指疫苗)。帖文附上網頁截圖及連結,指相關訊息來自文件的第3.4段「毒性結論」(Toxicity conclusions)。[4]

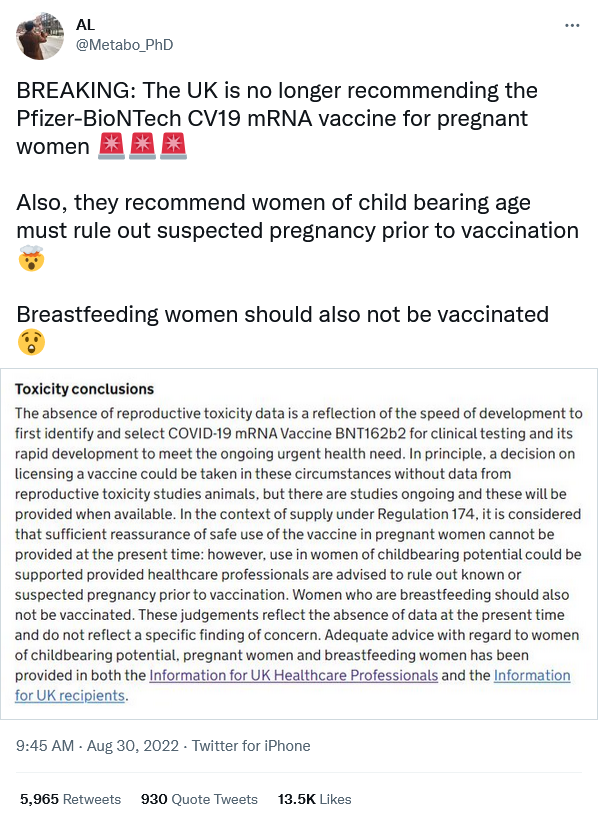
該組帖文亦有轉發來自另一Twitter用戶「AL」(@Metabo_PhD)的帖文,並附上網站「normanfenton.com」的文章連結。[5,6]「AL」帖文大部分宣稱與「Nikki」雷同,亦有「毒性結論」的截圖,並提及「英國建議育齡婦女在接種疫苗前必須排除懷孕可能」,該帖文有1.3萬個「喜歡」及近6,000次轉發。[7]
「Normanfenton.com」是倫敦大學瑪麗皇后學院(Queen Mary University of London)電子工程及資訊工程學院教授諾曼·芬頓(Norman Fenton)的個人網站。[8]
芬頓文章於8月29日刊登,提及曾經更新內文,現時版本引述3份聲稱來自英國政府的文件,並有以下宣稱[9]:
- 首份文件與上述「Nikki」帖文附載的英國政府網站連結相同。[10]芬頓引述文件來自Twitter用戶「Tracy2017」(@TracyK2017)帖文,指該文件於2022年8月16日更新,但帖文後來被人指正,因Wayback Machine備份記錄顯示網頁未有修改。他列出相關「毒性結論」涉及懷孕及哺乳婦女的內容,並質疑政府官員及國民保健署(National Health Services, NHS)建議孕婦接種疫苗,與該政府文件相違背;[11]
- 第二份文件同樣取自「Tracy2017」帖文[12],聲稱是與首份文件相似的備份版本[13],並引述文件稱「潛在益處大於對母親和胎兒的任何潛在風險時,才應考慮在妊娠期接種 COVID-19 mRNA疫苗 BNT162b2」;[14]
- 芬頓聲稱從已退休衛生保健人士取得的一份2020年12月由政府發出予英國相關業界專業人士的文件[15],他引述該文件提及:
- 不建議懷孕期間接種疫苗
- 育齡婦女在接種疫苗前應排除懷孕,接種第二劑後的兩個月內應避免懷孕
- 哺乳期間不應接種疫苗
- 未清楚疫苗會對生育能力有影響
除了引用上述Twitter用戶「Nikki」的帖文外,Facebook另有不同用戶轉載類似宣稱的內容,並加上標記「#網友發現英國政府悄悄修改接種復必泰指引」,並指資料來自「Nikki Miu國際新聞」及「NikkiMiu」。[16-18]其中一名用戶貼上Telegram頻道「Nikki Miu國際新聞台」訊息的連結[19],該訊息附有相同標記「#網友發現英國政府悄悄修改接種復必泰指引」,亦有「Tracy2017」Twitter帖文、聲稱為英政府網頁的截圖及芬頓網站連結。該訊息於8月30日發佈,有5,045人閱覽,頻道簡介為「無問責制翻譯新聞台」。[20]
查證
綜合上述多個流傳及轉發的訊息,查證報告會集中處理:
- 該批文件是否屬英國政府的接種疫苗指引?
- 英國政府有否更新或修改相關文件?
- 英國政府現時就懷孕、哺乳及育齡婦女的接種疫苗指引為何?
網傳訊息及供查證文件以「輝瑞/BioNTech COVID-19 疫苗」、「COVID-19 mRNA疫苗 BNT162b2」等用字稱呼相關疫苗。輝瑞及BioNTech共同研發的mRNA COVID-19疫苗,商品名為Comirnaty,代號為BNT162b2,中文名為復必泰,報告下文將以復必泰疫苗統稱。[21-23]
文件屬2020年底的初期報告
網絡於2022年8月底開始流傳聲稱為「英國政府網頁」的截圖及連結[24],檢視該資料在相關時段的網頁備份[25],文件為復必泰疫苗上巿評估報告摘要(Summary of the Public Assessment Report for COVID-19 Vaccine Pfizer/BioNTech),由英國藥物及保健產品規管局(Medicines & Healthcare products Regulatory Agency, MHRA)上載。根據MHRA資料,當局會就新獲批上巿的藥品發表相關科學評估報告,名為上巿評估報告。[26]報告摘要現時頁面與8月下旬版本相比,頁首新增說明解釋報告僅屬2020年12月批發許可時的初期評估報告。[27]
摘要列明,復必泰疫苗上巿評估報告由英國衛生及社會關懷部(Department of Health and Social Care)、輝瑞及BioNTech提供,主要用作解釋復必泰疫苗如何根據《人體藥物規例》第174條(Regulation 174 of the Human Medicine Regulations)進行評估、獲批許可及其產品的使用條件,並列明文件非使用疫苗的實務建議。[28]按英國法律網站,該條文列明若當局臨時批准許可予藥物以應對疑似或確認的病原體、毒素等傳播,另一針對藥物要求的條文則不適用。[29]
MHRA就復必泰疫苗的批准許可設有文件專頁,列出多份文件供專業人士及公眾參考。[30]綜合該頁及報告摘要的資料,復必泰疫苗於2020年12月1日獲臨時供應許可(Authorisation for the temporary supply)在英國上巿,至同月21日歐洲藥物管理局(European Medicines Agency, EMA)發出有條件的上巿許可(conditional Marketing Authorization),其後在2021年1月1日即自動轉變成在英國取得同類許可。所有現存的復必泰疫苗供應均有條件的上市許可,按照174條規定上巿的庫存將於2022年2月到期。[31]
網絡流傳的復必泰疫苗報告僅為2020年取得英國藥物監管機構臨時許可的資料,並非長期接種疫苗指引。
更新內容不涉懷孕哺乳資料
網傳訊息聲稱文件於2022年8月16日更新,設有「毒性結論」一欄。同年8月底的網頁備份顯示,文件標題下方列明「Updated 16 August 2022」,但內文則提及報告摘要曾於2021年6月更新。[32]
Wayback Machine最早於2020年12月16日備份該網頁[33],該記錄顯示當時報告摘要已有「毒性結論」一欄,內容與網傳時期及現時版本完全相同。[34]復必泰疫苗批准許可的文件專頁設有「See all updates」,點擊可看到各文件何時上載至網頁、何時更新及相關內容。該頁顯示,復必泰疫苗上巿評估報告全文在2020年12月15日上載至網站,翌日新增報告摘要,至2021年6月更新報告內的接種疫苗年齡。
對比2020年12月與2021年6月兩個版本,全文僅有三處修改,均亦與孕婦接種安全性無關。[35, 附錄]文件專頁亦顯示,2022年8月16日更新的文件為「復必泰疫苗產品特性」及「病人資料單張」,修改內容主要涉及疫苗加強劑及疫苗保質期等資料。[36]
換言之,復必泰疫苗上巿評估報告摘要並非於2022年8月16日更新,對上一次更新日期為2021年6月,修改的內容與婦女懷孕、哺乳及生育的資料完全無關,該部分內容自上載至網頁後亦未曾修改。
文件說法基於缺乏數據
網傳訊息關注報告摘要「毒性結論」一欄,惟參考該段完整文字[37],內文另提及:因要盡快選取復必泰疫苗進行臨床測試及加快研發以應對迫切的健康需求,故缺乏相關生殖毒性數據,但原則上仍可以批出疫苗許可,相關研究持續進行,若有數據將會提供。
該文指出基於174條規例性質(意指臨時授權),當時無法為孕婦安全接種疫苗提供足夠保證,建議育齡接種疫苗前排除懷孕可能,哺乳期間亦不應注射疫苗,並強調相關判斷僅反映目前缺乏數據,並非因為有研究發現疫苗不安全。
「毒性結論」刊於2020年12月發佈的報告摘要,當時復必泰疫苗僅獲臨時授權,未有相關生殖毒性數據,故提出懷孕、哺乳及育齡婦女應避免接種復必泰疫苗的說法,僅屬疫苗2020年底獲臨時批准使用時的建議,並非長期指引。
英政府21年建議孕婦及哺乳人士接種疫苗
在Google搜尋「COVID-19 vaccination pregnancy and breastfeeding UK」,可以找到由英國衛生安全局(UK Health Security Agency)發佈的懷孕及哺乳人士COVID-19疫苗接種指引。[38] 指引於2022年9月2日更新,對上一次更新日子顯示為同年4月,對照Wayback Machine備份記錄,兩者內容相同。[39]
指引引述英國疫苗接種和免疫聯合委員會(The Joint Committee on Vaccination and Immunisation, JCVI)意見,建議孕婦及哺乳人士接種COVID-19疫苗,又指首選(preferred)疫苗為復必泰或莫德納(Moderna)。
JCVI在2020年年底發表優先群組接種COVID-19疫苗建議,當中提及雖懷孕及哺乳期間接種非活疫苗(non-live vaccines)並無已知風險,但當時證據不足,故僅建議孕婦在有高度且不可避免風險會接觸及感染SARS-CoV2病毒、或感染後有嚴重併發症潛在風險的情況下接種COVID-19疫苗。[40]
2021年4月16日,JCVI就孕婦接種疫苗有新建議,新聞稿解釋建議的相關理據[41],因應美國疾病控制及預防中心(Centers for Disease Control and Prevention, CDC)資料顯示[42],當時已有9萬名孕婦接種COVID-19疫苗,主要為復必泰或莫德納,沒有引起安全疑慮,故建議英國孕婦同樣跟隨,並強調無證據顯示其他疫苗對孕婦不安全,只是仍然需要更多研究。至於計劃懷孕、產後或哺乳者可視乎其年齡及臨床風險選擇各款疫苗。JCVI稱孕婦接種疫苗建議已刊登至名為「Green Book」的疫苗臨床專業指南。[43]
數據及研究顯示疫苗對孕婦及哺乳無負面影響
英國MHRA設有Yellow Card機制,供醫療專業人士及大眾向當局匯報任何藥物或疫苗等引起的可疑副作用。[44]2022年9月MHRA就COVID-19疫苗的Yellow Card報告摘要指出[45],根據當局收到的報告,並未發現任何規律顯示英國使用的COVID-19疫苗或因對疫苗的反應而增加流產、死產、先天性異常或妊娠併發症的風險。[46]
Yellow Card摘要解釋,COVID-19疫苗與大部分疫苗及藥物的情況雷同,在大眾使用前並沒有在孕婦進行臨床測試,但現時有越來越多臨床使用數據為孕期疫苗安全性提供保證。[47]摘要同時列出多項大型研究結果,包括:
- 綜合一項美國涉及逾10萬次懷孕數據的研究及一項有逾1.8萬名孕婦的挪威研究,指研究發現未接種者與在3至5週內曾接種疫苗者的流產比率相若。[48,49]
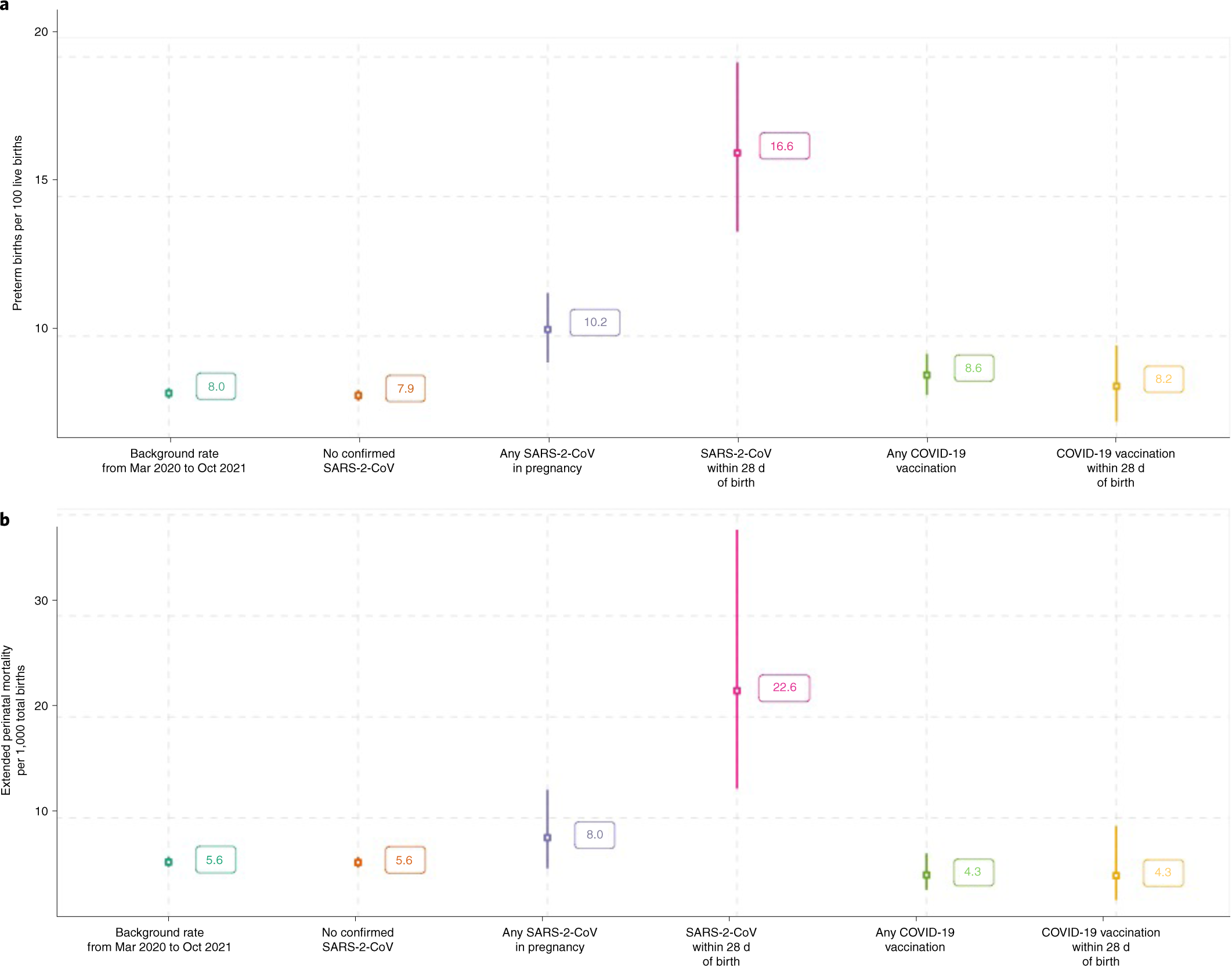
- 根據蘇格蘭國民保健署(Public Health Scotalnd)監察[50]及一項按當地數據在醫學期刊《自然醫學》(Nature Medicine)發表的研究[51]顯示,分別在懷孕及分娩期28日內接種疫苗者、未接種疫苗及無感染COVID-19的分娩者,其延長周產期死亡(extended perinatal mortality,包括妊娠24週以上在子宮內死亡及新生28日內死亡)比率相若(見圖8)。
- 引用一項已發佈的以色列大型研究,其中有逾2,000名孕婦在懷孕首三個月接種疫苗,同一時期有3,500名孕婦未有接種,研究發現兩者在早產率、新生嬰兒住院或死亡率、嬰孩先天缺陷比率並無差異。[52]
摘要指出,Yellow Card收到約4,000宗涉及接種疫苗期間餵哺母乳的報告,大部分報稱的懷疑疫苗反應與一般大眾的情況雷同,未有提及會對母乳供應及孩童的影響,目前亦沒有證據顯示疫苗對哺乳能力或進食母乳的孩童有任何傷害。[53]
2022年8月《刺針(傳染病)》雜誌(Lancet Infectious disease)發佈一則由美國CDC人員撰寫的評論文章,綜合同期刊登的一項加拿大大型研究與其他研究及監測數據,顯示孕婦期間接種COVID-19 mRNA疫苗屬安全。[54]
芬頓引用文件屬舊資料
網絡流傳的芬頓文章除了提及上述有關復必泰疫苗的報告撰要外,亦有引述聲稱屬英國政府的文件。第二份文件的標題為「就輝瑞/BioNTech COVID-19疫苗給予專業人士的資料(174條規定)」[55],但起首有「ARCHIVE」字眼註明文件已歸檔,即相關內容現時已不適用。
至於第三份聲稱來自退休衛生保健界人士的文件,該文件連結的域名為「filesusr.com」,並非來自官方網站,封面頁註明為「REG 174 INFORMATION FOR UK HEALTHCARE PROFESSIONALS」。[56]
搜尋該文件字眼,可以在MHRA就復必泰疫苗批准許的專頁找到相同標題的文件,同樣有「ARCHIVE」字眼註明文件已歸檔。[57,58]對比Wayback Machine最早於2020年12月就該文件的備份記錄,可以確定內容與芬頓文件完全相同。[59,60]
2022年5月,有社交媒體帖文宣稱該文件來自復必泰疫苗藥廠輝瑞,不建議孕婦接種疫苗。《法新社》(AFP)查證確認文件由MHRA在2020年12月發佈予衛生保健專業人士,MHRA發言人回覆稱,文件內容是當時的初期評估(assessment at the time),並不反映現時疫苗指引。因孕婦及哺乳人士一般都被剔除在早期的臨床測試,在有限數據的情況下英國初期並不推薦此類群體接種疫苗,至後來才更新相關指引建議相關人士接種。查核報告另引述多項研究及採訪專家說明COVID-19疫苗對孕婦的安全性及保護作用。[61]
芬頓文章引用的文件屬舊資料,現時已不適用。文件提到不推薦孕婦接種復必泰疫苗的說法,乃因早期缺乏相關臨床測試數據,英國政府後來已修改指引建議孕婦及哺乳人士接種疫苗,惟該文件曾被誤植為藥廠文件以質疑疫苗安全性。
在Google搜尋「UK covid vaccine pregnant factcheck」,亦可以找到多間外國傳媒及查核機構在2022年8月底開始就復必泰上巿評估報告摘要的內容發表查核報告及報導,確認英國官方近日並沒有更改指引至不建議懷孕及哺乳婦女接種COVID-19疫苗。[62-67]
結論
2022年8月底開始,網絡流傳聲稱來自英國政府網站截圖及連結,指當地於今年8月中修改接種復必泰疫苗指引,由原本顯示懷孕及哺乳婦女可接種,改為無法為孕婦安全使用提供足夠保證,哺乳婦女亦不應接種。
查證發現,該截圖及連結屬2020年12月復必泰在英國取得臨時上巿許可的相關文件,對上一次更新日期為2021年6月,並非今年8月,修改的內容亦與孕婦、哺乳等部分無關。文件非接種疫苗的長期指引,並註明就生育、懷孕及哺乳應否接種疫苗說法,只反映當時缺乏充分數據下的建議。
英國政府自2021年4月正式建議孕婦接種COVID-19疫苗,至今沒有修改該立場,並引用多項數據及研究說明疫苗對孕婦及哺乳無負面影響。網絡另流傳文章引述其他英國政府文件質疑孕婦接種疫苗安全性,經查證後確認為舊資料,現已不適用。
網傳訊息將英國政府舊資料稱為8月中更新疫苗指引,以該文件質疑婦女生育、懷孕及哺乳接種COVID-19不安全,屬錯誤訊息。
附錄
對比2020年12月(舊版)與2021年6月(新版)兩個版本的復必泰疫苗上巿評估報告摘要,全文三處修改於下(改動處以粗體顯示):
1. Lay summary, “What is BNT162b2 and what is it used for?”
舊版︰BNT162b2 is a vaccine indicated for active immunisation of individuals 16 years of age and older to prevent COVID-19 caused by the SARS-CoV-2 virus.
新版︰BNT162b2 is a vaccine indicated for active immunisation to prevent COVID-19 caused by the SARS-CoV-2 virus, in individuals 12 years of age and older.
2. Lay summary, “Other information about BNT162b2”
舊版︰This summary was last updated 11 December 2020.
新版︰This summary was last updated in June 2021. 另新增此句:A marketing authorisation was granted for the Pfizer/BioNTech vaccine (Comirnaty) following a European Commission (EC) decision on 21 December 2020 (PLGB 53632/0002).
3. Lay summary, 1. Introduction
新版加上此句︰On 4 June 2021 the MHRA granted an extension of indication to ‘the active immunisation to prevent COVID-19 caused by the SARS-CoV-2 virus, in individuals 12 years of age and older’.
資料來源
- Facebook專頁「白兵 Stormtrooper」帖文
- Twitter用戶「Nikki」(@nikki_miumiu)帖文
- Facebook用戶「SauWai Chan」帖文
- Summary of the Public Assessment Report for COVID-19 Vaccine Pfizer/BioNTech (Medicines & Healthcare products Regulatory Agency)
- Twitter用戶「AL」(@Metabo_PhD)帖文
- BREAKING NEWS: UK Government website says vaccine not safe for pregnant or breastfeeding women (Norman Fenton)
- 見[5],「Also, they recommend women of child bearing age must rule out suspected pregnancy prior to vaccination」。
- About Me (Norman Fenton)
- BREAKING NEWS: UK Government website says vaccine not safe for pregnant or breastfeeding women (Norman Fenton) Wayback Machine於2022年9月9日的網頁備份
- 文件連結與[4]相同。
- 見[6],原文為”However, this would make things even worse as it means that the Government officials and the NHS have been recommending pregnant women get the vaccine against the official Government document advice”。
- Twitter用戶「Tracy2017」(@TracyK2017)帖文,查核期間Twitter指該文來自遭停用的帳戶,暫無法顯示相關內容。
- ARCHIVE: Information for Healthcare Professionals on COVID-19 Vaccine Pfizer/BioNTech (Regulation 174) (Medicine & Healthcare products Regulatory Agency)
- 見[6]及[12],原文為”Administration of the COVID-19 mRNA Vaccine BNT162b2 in pregnancy should only be considered when the potential benefits outweigh any potential risks for the mother and foetus.”。
- Reg 174 Information for UK Healthcare Professionals
- Facebook用戶「Ng Mrnmy」於群組「被迫打針關注組」帖文
- Facebook用戶「JJ Ho」帖文
- Facebook用戶「Coco Law」於群組「復必太針後康復關注組 (香港)」帖文
- Telegram頻道「Nikki Miu國際新聞台」訊息
- Telegram頻道「Nikki Miu國際新聞台」
- 关于使用被列入紧急使用列表的辉瑞–BioNTech COVID-19疫苗BNT162b2的临时建议(世界衛生組織)
- 輝瑞/BioNTech疫苗 你需要了解的幾個問題(BBC News中文)
- 复星医药和BioNTech共同宣布 mRNA新冠疫苗于中国香港获紧急使用认可(復星醫藥)
- 見[1]、[2]、[3]、[5]、[6]及[16-19]。
- Summary of the Public Assessment Report for COVID-19 Vaccine Pfizer/BioNTech (Medicines & Healthcare products Regulatory Agency) Way Machine於2022年8月27日的網頁備份
- Find product information about medicines (Medicines & Healthcare products Regulatory Agency)
- 見[4]及[25],現時版本的頁面新增灰框說明,原文為“The Public Assessment Report summarises the initial assessment at the time of approval in December 2020.”。
- 見[25],在“Lay summary, COVID-19 mRNA Vaccine BNT162b2 concentrate for solution for injection (BNT162b2 RNA)”標題下,原文為“It explains how this product was assessed and authorised under Regulation 174 of the Human Medicine Regulations, as well as its conditions of use. It is not intended to provide practical advice on how to use this product.”。
- Section 174, The Human Medicines Regulations 2012 (legislation.gov.uk),174條另提及46條就批准藥物許可的要求。
- Regulatory approval of Pfizer/BioNTech vaccine for COVID-19 (Medicines & Healthcare products Regulatory Agency)
- 見[25]及[30],[25]資料見於小標題“Other information about BNT162b2”。
- 見[25],原文為“This summary was last updated in June 2021.”。
- Summary of the Public Assessment Report for COVID-19 Vaccine Pfizer/BioNTech (Medicines & Healthcare products Regulatory Agency) Way Machine於2020年12月16日的網頁備份
- 見[4]、[25]及[29]有關Toxicity conclusions的內容。
- Summary of the Public Assessment Report for COVID-19 Vaccine Pfizer/BioNTech (Medicines & Healthcare products Regulatory Agency) Way Machine於2020年12月16日的網頁備份
- 見[30],原文為16 August 2022, Updates to the SmPC and PIL to include information about receiving a heterologous booster dose in individuals aged 18 years and over. Updated SmPC and PIL for the purple cap product (Comirnaty 30 micrograms/dose concentrate for dispersion for injection) – shelf life and transportation storage time information updated.”。見[26],SPC為Summary of Product Characteristics,PIL為Patient Information Leaftlet。
- 見[34],原文為“The absence of reproductive toxicity data is a reflection of the speed of development to first identify and select COVID-19 mRNA Vaccine BNT162b2 for clinical testing and its rapid development to meet the ongoing urgent health need. In principle, a decision on licensing a vaccine could be taken in these circumstances without data from reproductive toxicity studies animals, but there are studies ongoing and these will be provided when available. In the context of supply under Regulation 174, it is considered that sufficient reassurance of safe use of the vaccine in pregnant women cannot be provided at the present time: however, use in women of childbearing potential could be supported provided healthcare professionals are advised to rule out known or suspected pregnancy prior to vaccination. Women who are breastfeeding should also not be vaccinated. These judgements reflect the absence of data at the present time and do not reflect a specific finding of concern. Adequate advice with regard to women of childbearing potential, pregnant women and breastfeeding women has been provided in both the Information for UK Healthcare Professionals and the Information for UK recipients.”
- COVID-19 vaccination: a guide on pregnancy and breastfeeding (UK Health Security Agency)
- COVID-19 vaccination: a guide on pregnancy and breastfeeding (UK Health Security Agency) Wayback Machine於2022年9月2日 07:39 網頁備份
- Joint Committee on Vaccination and Immunisation: advice on priority groups for COVID-19 vaccination, 30 December 2020 (Department of Health and Social Care)
- JCVI issues new advice on COVID-19 vaccination for pregnant women (Public Health England)
- V-safe COVID-19 Vaccine Pregnancy Registry (Centers for Disease Control and Prevention) Wayback Machine於2021年4月16日的網頁備份
- COVID-19: the green book, chapter 14a (UK Health Security Agency)
- Welcome to the Yellow Card reporting site (Medicines & Healthcare products Regulatory Agency)
- Coronavirus vaccine - summary of Yellow Card reporting (Medicines & Healthcare products Regulatory Agency)
- 見[45],原文“There is no pattern from the reports to suggest that any of the COVID-19 vaccines used in the UK, or any reactions to these vaccines, increase the risk of miscarriage, stillbirths, congenital anomalies or birth complications.”。
- 見[45],原文為“Although, like most vaccines and medicines, clinical trials of COVID-19 vaccines in pregnant women were not carried out prior to use of the vaccines in the general population, there is now growing evidence from clinical use which provides reassurance on the safety of the vaccines in pregnancy.”
- Kharbanda EO, et al. Spontaneous abortion following COVID-19 vaccination during pregnancy. JAMA. doi:10.1001/jama.2021.15494.
- Magnus, MC et al. Covid-19 Vaccination during Pregnancy and First-Trimester Miscarriage. N Engl J Med 2021; 385:2008-2010 DOI: 10.1056/NEJMc2114466.
- COVID-19 statistical report (Public Health Scotland)
- Stock SJ, et al SARS-CoV-2 infection and COVID-19 vaccination rates in pregnant women in Scotland Nature Medicine 2022
- Goldshtein et al Association of BNT162b2 COVID-19 Vaccination During Pregnancy With Neonatal and Early Infant Outcomes JAMA Pediatrics (2022) doi:10.1001/jamapediatrics.2022.0001
- 見[45],小標題Safety of COVID-19 vaccines in those breastfeeding”下的內容。
- Ellington S, Olson C K Safety of mRNA COVID-19 vaccines during pregnancy Lancet Infectious Disease doi:10.1016/S1473-3099(22)00443-1
- 見[13]。
- 見[15]
- 見[30],該文件標題為“ARCHIVE: Information for Healthcare Professionals on COVID-19 Vaccine Pfizer/BioNTech (Regulation 174)”。
- Reg 174 Information for UK Healthcare Professionals (Medicines & Healthcare products Regulatory Agency)
- Reg 174 Information for UK Healthcare Professionals (Medicines & Healthcare products Regulatory Agency) Wayback Machine於2020年12月5日的網頁備份
- 見[15]及[59]。
- Posts falsely claim Pfizer Covid-19 vaccine dangerous during pregnancy (AFP Factcheck)
- Fact Check-Britain's MHRA still advises pregnant and breastfeeding women to get vaccinated against COVID-19 (Reuters)
- UK didn’t change guidance on COVID vaccines and pregnancies (AP News)
- Outdated report misconstrues UK’s COVID-19 vaccine guidance around pregnancy (Politifact)
- Pregnant and breastfeeding women are still advised to get the Covid-19 vaccine (Full Fact)
- Fact Check: Has Advice On Pfizer Vaccine Use During Pregnancy Changed? (Newsweek)
- UK did not change Covid-19 vaccination guidance for pregnant people (AFP Factcheck)
